只有单细胞转录组数据的肿瘤类器官研究(肝癌)
虽然早在2009年,荷兰Hubrecht研究所的Hans Clevers博士就证实 肠干细胞 能够形成类器官,开启了 类器官研究的时代。但是早期类器官并没有在肿瘤领域大放异彩,算起来单细胞也是2009年汤富酬博士开启的,但是也是在发育生物学领域“小步慢跑”。
我常见系统性梳理过 2014到2018期间的癌症领域的单细胞研究,可以说是少得可怜,都是broad研究所的基于smart-seq的,在脑瘤,黑色素瘤,头颈癌有CNS文章发表。同样的是这个时间段, 类器官也是在每个癌症领域都有了CNS文章,比如 :
- 2018的cell杂志:《Generation of Tumor-Reactive T Cells by Co-culture of Peripheral Blood Lymphocytes and Tumor Organoids》
- 2018的cell杂志:《A Living Biobank of Breast Cancer Organoids Captures Disease Heterogeneity》
- 2018的Cancer Discovery杂志:《Organoid profiling identifies common responders to chemotherapy in pancreatic cancer》
- 2018的cell杂志:《Tumor Evolution and Drug Response in Patient-Derived Organoid Models of Bladder Cancer》
- 2018的Cell Stem Cell:《A Comprehensive Human Gastric Cancer Organoid Biobank Captures Tumor Subtype Heterogeneity and Enables Therapeutic Screening》
有意思的是2019年开始,标准化的10x的单细胞转录组商品化大大获成功让单细胞转录组走入了几乎每个课题组,而类器官缺受限于实验细节繁琐一直“不温不火”,早期的在每个癌症领域的类器官CNS文章都是做几十个或者上百个病人的类器官培养后,做常规的转录组和肿瘤外显子数据,来说明类器官能非常好的维持其来源的原位肿瘤,这样就说明了类器官可以成为肿瘤病人的精准医疗替身!
但是早期的在每个癌症领域的类器官CNS文章已经是非常一致的展现了类器官培养的成功率,常规的转录组和肿瘤外显子层面的异质性,药物反应情况,以至于后面的研究没办法做下去了。恰好单细胞时代到了,可以让2019之后的类器官研究继续“复制粘贴一波”,比如2021发表Advanced Science期刊的类器官文章:《Single-Cell Transcriptome Analysis Uncovers Intratumoral Heterogeneity and Underlying Mechanisms for Drug Resistance in Hepatobiliary Tumor Organoids》,就已经舍弃了传统的常规的转录组和肿瘤外显子数据,仅仅是看单细胞转录组。
因为 Hepatobiliary Tumor是上皮来源的肿瘤,所以原则上成功培养后的类器官里面就是纯粹的上皮细胞,没办法走我们推荐的单细胞转录组降维聚类分群和命名流程,通常我们拿到了肿瘤相关的单细胞转录组的表达量矩阵后的第一层次降维聚类分群通常是:
- immune (CD45+,PTPRC),
- epithelial/cancer (EpCAM+,EPCAM),
- stromal (CD10+,MME,fibro or CD31+,PECAM1,endo)
参考我前面介绍过 CNS图表复现08—肿瘤单细胞数据第一次分群通用规则,这3大单细胞亚群构成了肿瘤免疫微环境的复杂。绝大部分文章都是抓住免疫细胞亚群进行细分,包括淋巴系(T,B,NK细胞)和髓系(单核,树突,巨噬,粒细胞)的两大类作为第二次细分亚群。但是也有不少文章是抓住stromal 里面的 fibro 和endo进行细分,并且编造生物学故事的。
因为类器官就是培养的恶性肿瘤上皮细胞,所以第一层次降维聚类分群后仍然是上皮细胞,而且是具有病人特异性的,如下所示:
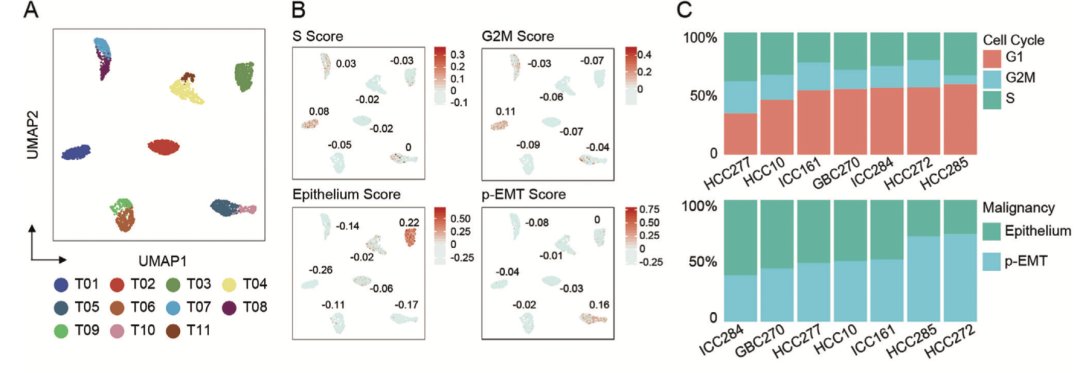
第一层次降维聚类分群
文章主要关注的是 three liver CSC-like markers (PROM1, EPCAM, and CD44) ,所以可以区分一下干性与否的二分组,然后就可以做差异分析:
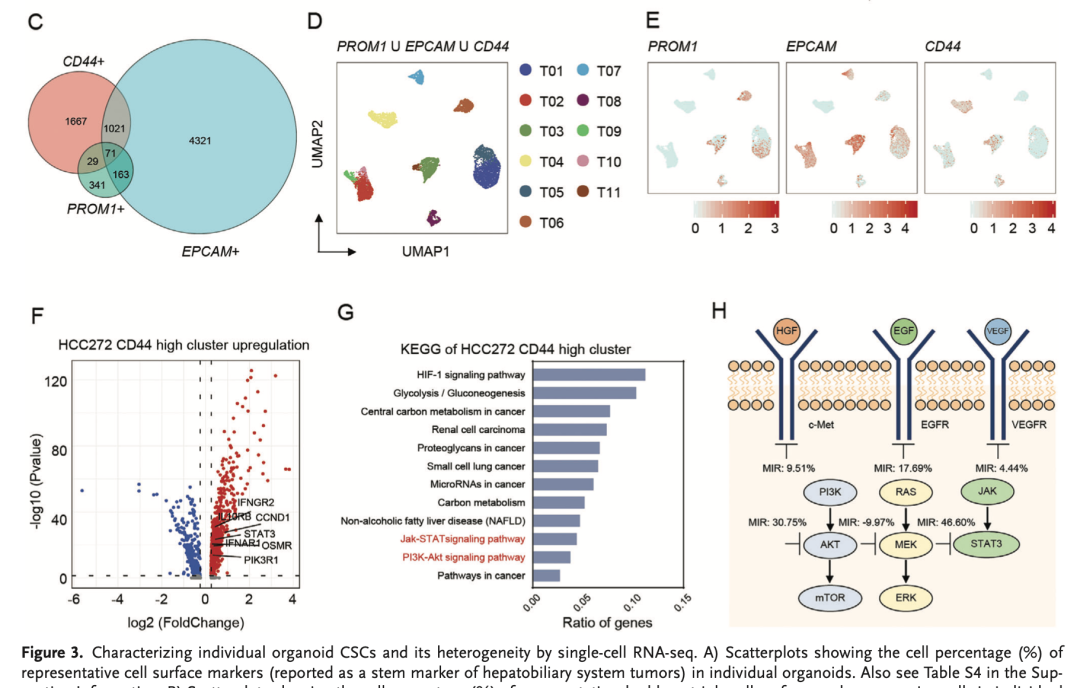
干性与否的二分组差异分析
因为单细胞转录组会在每个病人产出成百上千个细胞,所以还可以看异质性,每个病人内部降维聚类分群后看特征基因,做拟时序分析看变化趋势:
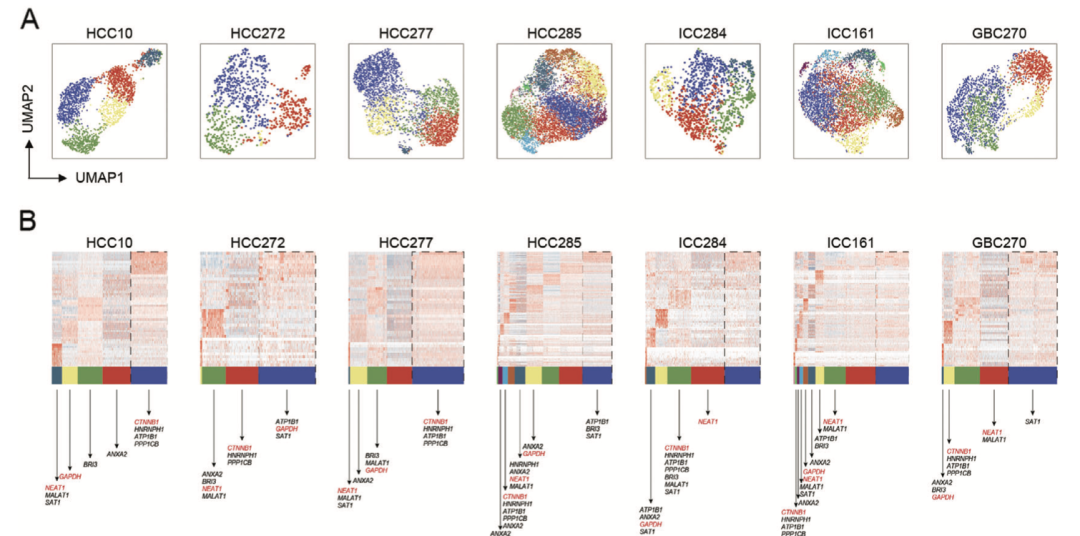
每个病人内部降维聚类分群后看特征基因